目的:为了进一步阐明一些营养补充剂对膝关节病的疗效和安全性,我们进行了一项初步的随机多中心(n=9)观察性研究,比较了Fortigel联合治疗的效果®(10克)和岩藻糖聚糖(100毫克)(ACTEN®),而另一种常用的治疗制剂基于葡萄糖胺(500毫克)、硫酸软骨素(400毫克)、透明质酸(50毫克)和维生素C(100毫克)(COMBIART)。
患者及方法:该方案在年龄40-65岁,诊断为轻度至中度膝关节骨关节炎(Kellgren Lawrence分级2-3级)的人群(n=126)中进行了为期12周的治疗。通过密切监测不良事件来衡量安全性。在基础、1个月和3个月的对照中,通过视觉模拟量表(VAS)和骨关节炎严重程度Lequesne疼痛功能指数(LAI)的关节功能分级评估来衡量疗效。
结果:两组在T1 (28.5% ACTEN)时的平均视觉模拟量表值均显著降低(P < 0.0001)®1个月时,COMBIART为21.3%,ACTEN为49.4%®3个月时,COMBIART为40.1%),Lequesne算法功能指数均值显著降低(P < 0.0001) (ACTEN®t1 28.9%, t3 44.9%,联合t1 21.3%, t3 37%)。效果似乎与时间有关,因为从T1到T2,两个参数的平均值进一步下降(P < 0.0001,对于两组的VAS;ACTEN的P为0.0011®对照组为LAI)。两组间无统计学差异®和COMBIART组在T1或T3时间。这些有趣的初步数据将在更大的范围内得到进一步的研究。
结论:Fortigel®(10克)和岩藻糖聚糖(100毫克)(ACTEN®)作为口服营养补充剂对膝关节骨性关节炎的治疗干预有显著影响,在治疗过程中VAS和LAI值显着下降。在COMBIART组中也证实了类似的效果,两组之间没有统计学上的显著差异。
骨关节炎(OA)是一种非常常见的缓慢进展的关节疾病,在成年人中引起明显的不适和残疾。这种情况的患病率随着年龄的增长而增加,众所周知的危险因素如遗传、肥胖、局部创伤和职业。25-35岁的成年人中有1%出现膝关节OA的重要影像学改变,而75岁及以上的老年人中这一比例几乎增加到50%。髋关节和膝关节骨关节炎是成年人中最常见的疾病。
骨关节炎具有炎症成分和组织破坏成分,导致这些关键的负重关节疼痛和僵硬[1]。这通常会造成严重的残疾,导致日常生活中进行正常活动的困难增加,在最严重的情况下需要进行关节置换手术。
对乙酰氨基酚和非甾体抗炎药(NSAIDs)是骨关节炎患者在日常严重情况下应对疼痛和僵硬的常用治疗方法。出于这个原因,近年来许多研究集中在替代分子和营养补充剂作为治疗选择,以实现软骨组织修复,同时绕过环氧化酶2 (COX-2)抑制剂和其他非甾体抗炎药的负面影响。葡萄糖胺已被广泛研究[2-18],在疼痛的临床治疗和结构改善方面显示出积极的结果[19]。硫酸软骨素与氨基葡萄糖偶联或单独使用已成为重要研究的中心[20],但也研究了许多其他合成或天然化合物,包括维生素C[21-25]。人们对胶原蛋白水解物(CHs)和岩藻多糖特别感兴趣[26-44]。CH是通过酶解哺乳动物胶原组织获得的。CH的主要特点是其氨基酸组成与II型胶原相同,因此提供高水平的甘氨酸和脯氨酸,这是软骨稳定和再生所必需的氨基酸[28]。本产品被监管机构认定为安全的食品成分。CH被很好地消化,并优先积聚在软骨中[29]。除了一些胃肠道副作用,如饱腹感或不愉快的味道外,临床使用CH与不良反应无关。
另一方面,岩藻聚糖是一类硫酸盐酸化的富含聚焦物的聚合物,存在于几种棕色巨藻中[41,42],用于各种不同的医疗条件[38]。最近的几项研究表明岩藻糖聚糖在解决骨关节炎症状中的作用。胶原诱导关节炎的动物模型显示,口服岩藻胶可成功抑制疼痛[39]。在一项小型人体临床研究中,口服富含岩藻多糖的海藻提取物12周后,骨关节炎症状被抑制了52%[40]。作为炎症标志物的TNF α没有降低,但在健康志愿者中进行的一项伴随研究显示,慢性炎症标志物白细胞介素6 (Interleukin 6)降低[43]。岩藻多糖对疼痛的影响与其选择性阻断中性粒细胞积累有关[44,45]。
为了检验这些化合物联合使用的临床疗效,CH (Fortigel®10克)和岩藻糖聚糖(100毫克)(ACTEN®),我们设计了一个初步的多中心随机临床试验。对照另一种临床使用的配方,测试其临床疗效,该配方基于众所周知的物质:葡萄糖胺(500mg)、硫酸软骨素(400mg)、透明质酸(50mg)和维生素C (100mg) (COMBIART)。
本试验设计为随机初步研究。该研究由一个研究小组在2015年10月至2016年5月期间在9个中心(意大利的拉齐奥和撒丁岛地区)进行,为期12周(84天),涉及126名年龄在40-65岁之间,患有轻度至中度膝关节骨关节炎(Kellgren Lawrence分级表2-3级)的参与者。
1)在研究开始时年龄在39岁或以下的个体被排除在研究之外;2)患有类风湿或其他形式的关节炎;3)因神经或肌肉损伤、意外、跌倒、创伤等导致关节疼痛(4)有通常与骨关节炎相关的合并症,如糖尿病、心血管疾病、需要医疗干预的胆固醇升高、肾功能不全、哮喘或需要医疗干预的高血压;5) 5年内患过癌症;6)正在服用任何其他草药产品或其他用于关节健康疼痛或炎症的补充剂,如葡萄糖胺/软骨素/甲基磺酰甲烷,s -腺苷蛋氨酸或omega-3;7)吸烟者;8)重度饮酒者;9)孕妇或哺乳期妇女;10)对贝类过敏;11) BMI低于18.5(体重不足)或大于40.0(病态肥胖)或体重超过225磅(102公斤)。 The demographics of the patient population are listed in Table 1.
表1。患者的人口统计数据。
人口 |
|
|
年龄 |
平均57.10 |
SD 8.04 |
男人 |
48 |
|
女性 |
78 |
|
脉管厘米 |
平均6.595 |
SD 1.318 |
LAI (Lequesne指数) |
平均10.595 |
SD 3.519 |
干预
参与者经历了为期四周的洗脱期,在此期间,他们停止服用所有针对骨骼、关节和炎症的膳食补充剂以及非处方药。
允许使用与关节健康无关的处方药,也允许只在需要时服用的非处方药。参与者还被要求在为期四周的试验中不要改变他们生活的任何方面。生活方式变量没有改变,包括但不限于饮食、健身方案、工作和家庭相关任务。
在基线预约时通过初步筛选的参与者被提供两种随机分配的营养补充剂(ACTEN)中的一种®或COMBIART),视觉模拟量表(VAS)问卷和Lequesne算法功能指数(LAI)的纸质副本。每位参与者被要求填写基线VAS和LAI问卷,并在开始服用补充剂之前将其交还给研究者。在第一个月,两组患者每天都服用补充剂。剩余8周ACTEN®一组每隔一天服用一次补充剂,而COMBIART每天继续服用。
在第1个月和第3个月(12周)再次收集数据。选择这种方法是为了反映凝胶(ACTEN)的高吸收率®)与胶囊相比(COMBIART)[46]。
结果测量
采用0 ~ 10分疼痛评分VAS, 0 ~ 24分疼痛和功能评分LAI,分别在补充4周和12周前后对两项指标进行评价。VAS评分是通过要求参与者在一条10厘米的线上标记反应来报告的。这条线包含两个终点锚点和3个额外的描述符,这些描述符沿VAS量表均匀间隔2.5 cm,以帮助确定参与者的方向。表2列出了每个尺度描述符的定义。
表2。VAS量表的内部描述符,LAI的描述符与先前发布的一样[45]。
VAS值(cm) |
疼痛程度 |
0 |
没有一个 |
2.5 |
温和的 |
5 |
温和的 |
7.5 |
严重的 |
10 |
坏的 |
在基线评估时,参与者被告知,如果在补充期间发生任何轻度、中度或严重的不良事件,应立即通知研究小组。在1个月的随访期间和3个月的随访期间,再次询问参与者在补充期间是否经历过任何不良事件或需要任何形式的救援治疗(疼痛或抗炎药)。没有投诉报告。
轻度、中度和严重不良事件的标准如下:(1)轻度:不良事件不影响日常活动,不需要特殊干预或治疗;(2)中度:不良事件可影响日常活动,且可通过简单治疗解决;(3)严重:需要治疗干预的不良事件。
统计分析
从VAS和LAI问卷中收集的数据采用双尾配对统计分析t对照两种治疗的T1(1个月)和T2(3个月)进行基线测试。采用双尾非配对t检验对数据进行交叉分析,比较疗效。使用Graphpad PRISM统计分析软件5.0版(La Jolla, CA, USA)进行分析。表示统计学显著性的alpha值为0.05。
在126名参加研究的参与者中,没有人因医疗并发症或不遵守研究方案而退出或被取消。与基线相比,所有参与者在4/12周结束时的所有测量结果具有统计学意义。的ACTEN®1个月(T1)时,患者关节疼痛减轻28.5%,VAS评分从基线时的6.68分(1.38SD)降至4.77分(1.98SD) (P= 0.0001;95% CI, 1.57, 2.25), T3时为-49.4%,平均VAS 3.38 (1.78SD) (P= 0.0001;95% ci, 2.95, 3.65)。LAI在T1时也下降了-28.9%,从平均基线11.28 (3.69SD)降至8.01 (P= 0.0001;95% CI, 2.72, 3.82), T3平均LAI为6.21 (3.01SD)时为-44.9% (P= 0.0001;95% ci, 4.42, 5.71)。
COMBIART组关节疼痛减轻21.3%,从基线时的平均VAS评分6.5 (1.25SD)降至T1时的5.11 (1.53SD)。P= 0.0001;95% CI, 1.09, 1.69)和- 40.1%的T3平均VAS 3.89 (1.81SD) (P= 0.0001;95% ci, 2.97, 4.33)。在T1时,LAI再次从平均基线9.84 (3.18 SD)减少到7.74 (3.08 SD),减少了-21.3% (P= 0.0001;95% CI, 1.63, 2.57),在T3时-37%,平均LAI为6.19 (3.04 SD) (P= 0.0001;95% ci, 2.97, 4.33)
的ACTEN®组似乎比COMBIART组更有效(VAS T3均值-49.4%/-40.1%;LAI T3均值为-44.9%/-37%),但两组比较无统计学意义[图1-4]。
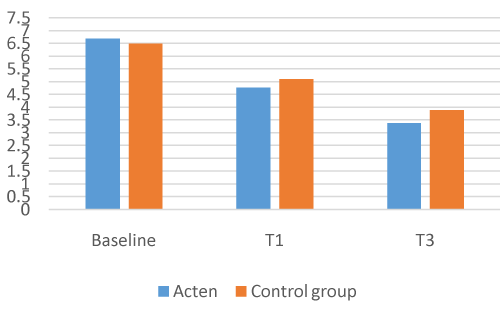
图1所示。VAS活跃组与对照组。
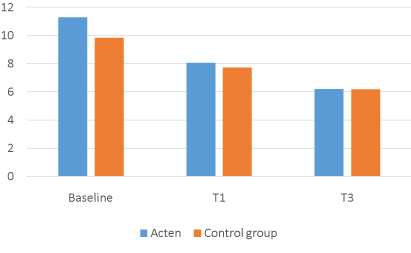
图2。Lequesme Index Acten vs COMBIART。
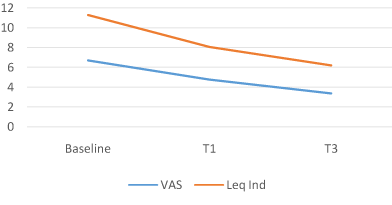
图3。ACTEN组。
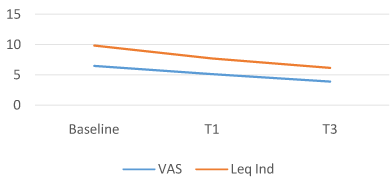
图4。COMBIART组。
不良反应摘要
研究期间未发现不良反应。
版权所有OAT。版权所有
骨关节炎是意大利和美国最常见的关节炎[47]。氨基葡萄糖、硫酸软骨素和透明质酸是存在于软骨细胞内和周围的天然物质,因此是OA和关节疼痛最常用的天然补充剂。先前的研究发现它们对于治疗OA的症状是有效和安全的[48,49]。特别是,2006年由美国国立卫生研究院(NIH)赞助的氨基葡萄糖/软骨素关节炎干预试验发现,与安慰剂相比,氨基葡萄糖联合硫酸软骨素对一部分参与者的疼痛缓解具有统计学意义[20]。
在这项研究中,我们评估了ACTEN的临床安全性和有效性®(CH 10gr, focuse 100 mg),并根据葡萄糖胺、硫酸软骨素、透明质酸和维生素C的附加值等已被充分研究的效果,将其与补充剂(COMBIART)进行比较[21]。正如预期的那样,COMBIART组在疼痛和功能指标上显着降低。疼痛和功能的减少在治疗的前4周就已经确定(VAS和LAI均为-21.3%),并在接下来的几周进一步增加,在T3(12周)时VAS和LAI分别达到-40.1%和-37%。ACTEN®结果相似,T1时VAS和LAI分别下降28.5%和28.9%。同样,长时间暴露达到最高疗效,在T3时VAS达到-49.4%,LAI达到-44.9%。尤其是ACTEN®组后8周仅每隔一天补充一次营养,未见疗效损失。两组之间没有统计学上的相关差异,但大量或长时间服用补充剂可能会发现细微的差异。
必须考虑到,每天服用ACTEN®,而不是在本试验中使用的每隔一天的方案,它可能会产生进一步的好处,应该进行调查。
两种营养补充剂(ACTEN)®和COMBIART)是安全的,耐受性良好,并且能够发挥重要的疼痛减轻和改善膝关节OA的功能。需要进一步的研究来确定其在减轻疼痛方面的疗效,并通过放射学研究来检查关节功能改善背后的结构变化。
- 李丽娟,刘建平,李建平,等(2013)骨关节炎的流行病学研究。Br Med Bull105: 185 - 199。(Crossref)
- 杨建军,陈建军,陈建军,陈建军(2005)氨基葡萄糖治疗骨关节炎的临床研究进展。公牛医院63: 31-36。(Crossref)
- Largo R, Alvarez-Soria MA, Diez-Ortego I, Calvo E, Sanchez-Pernaute O等。(2006)葡萄糖胺抑制il -1 β诱导的人骨关节炎软骨细胞NFkappaB活化。Osteoarthr Cartil11: 290 - 298。
- Alvarez-Soria MA, Largo R, Calvo E, Herrero-Beaumont G(2005)硫酸氨基葡萄糖与其他抗骨关节炎药物对培养的人类骨关节炎软骨细胞和滑膜成纤维细胞的不同抗代谢谱。Osteoarthr Cartil13: S153。
- Uitterlinden EJ, Jahr H, Koevoet JL, Jenniskens YM, Bierma-Zeinstra SM,等。(2006)葡萄糖胺降低人骨关节炎软骨移植体合成代谢和分解代谢基因的表达。Osteoarthr Cartil14: 250 - 257。
- Taniguchi S, Ryu J, Seki M, Sumino T, Tokuhashi Y等。(2012)长期口服葡萄糖胺或硫酸软骨素可减少自发性骨关节炎模型中软骨的破坏和MMP-3 mRNA的上调。J骨科30: 673 - 678。(Crossref)
- 李建军,李建军,李建军,等。(2011)氨基葡萄糖和NF-kB抑制剂对骨性关节炎的表观遗传影响。生物化学,生物物理学,公共科学405: 362 - 367。
- Altman RD, Abramson S, Bruyere O, Clegg D, Herrero-Beaumont G等。(2006)评论:膝关节骨关节炎与葡萄糖胺。Osteoarthr Cartil14: 963 - 966。
- 李建军,刘建军,刘建军,等(2007)氨基葡萄糖在骨性关节炎治疗中的作用。风湿病学(牛津)46: 731 - 735。(Crossref)
- 王晓明,王晓明,王晓明,王晓明,等(1994)膝关节骨性关节炎肌内注射硫酸氨基葡萄糖的疗效和安全性。一项随机、安慰剂对照、双盲研究。Arzneimittelforschung44: 75 - 80。(Crossref)
- 陈志强,陈志强,陈志强(1993)葡萄糖胺在人体中的药代动力学研究。Arzneimittelforschung43: 1109 - 1113。(Crossref)
- Leffler CT, Philippi AF, Leffler SG, Mosure JC, Kim PD(1999)葡萄糖胺、软骨素和抗坏血酸锰治疗膝关节或腰背部退行性关节疾病:随机、双盲、安慰剂对照的初步研究。军医164: 85 - 91。(Crossref)
- Rovati L .(1997)硫酸氨基葡萄糖选择性治疗骨关节炎的临床研究。Rheumatol欧元pp: 26:70。
- 胡文杰,陈建平,陈建平,等(1999)盐酸氨基葡萄糖治疗膝关节骨性关节炎疼痛的疗效观察。J Rheumatol26日:2423 - 2430。(Crossref)
- Rovati L(1993)硫酸氨基葡萄糖治疗脊柱骨关节炎的临床疗效。Rev(尤指Reumatol20 (S1): 325。
- m ller- fassbender H, Bach GL, Haase W, Rovati LC, Setnikar I(1994)硫酸氨基葡萄糖与布洛芬治疗膝关节骨性关节炎的比较。骨关节炎软骨2: 61 - 69。(Crossref)
- 邱广祥,高士生,陈建平,陈建平(1998)硫酸氨基葡萄糖与布洛芬治疗膝关节骨性关节炎的疗效与安全性。Arzneimittelforschung48: 469 - 474。(Crossref)
- Rovati L(1997)硫酸氨基葡萄糖作为选择性改善骨关节炎症状的药物的临床概况:目前的数据和观点。Osteoarthr Cartil5 (SA): 72。
- 李建军,刘建军,李建军,刘建军,等(2012)骨关节炎的临床研究进展。Rheumatol Int32: 2959 - 2967。(Crossref)
- Clegg DO, Reda DJ, Harris CL, Klein MA, O'Dell JR等。(2006)氨基葡萄糖、硫酸软骨素联合治疗膝关节骨性关节炎。[英]医学354: 795 - 808。(Crossref)
- Peregoy J, Wilder FV(2011)补充维生素C对发生和进展性膝骨关节炎的影响:一项纵向研究。公共卫生营养14: 709 - 715。(Crossref)
- Malek Mahdavi A, Mahdavi R, Kolahi S, Zemestani M, Vatankhah AM。补充左旋肉碱可改善女性膝关节骨性关节炎患者的临床状况,但不改变氧化应激和脂质特征。减轻35: 707 - 715。
- 黄柏提取物对骨性关节炎患者关节健康的影响:一项前瞻性、双盲、安慰剂对照研究。减轻J38。
- Witt CM, Michalsen A, Roll S, Morandi A, Gupta S等。(2013)综合阿育吠陀治疗与常规标准护理治疗膝关节骨性关节炎的疗效比较。随机对照试验的研究方案。试用14: 149。
- 叶崎杰,梁志强,梁志强,等。(2013)甲基磺酰甲烷对骨关节炎动物模型骨和膝关节的安全性和有效性评价。J骨矿工Metab第16 - 25:31。(Crossref)
- McAlindon TE, Nuite M, Krishnan N, Ruthazer R, Price LL等。(2011)水解胶原蛋白治疗后延迟钆增强磁共振成像检测膝关节骨性关节炎软骨的变化:一项随机对照试验。骨关节炎软骨19日:399 - 405。(Crossref)
- Bannuru RR, Osani M, Vaysbrot EE, McAlindon TE(2016)透明质酸产品治疗膝关节骨性关节炎的安全性比较:系统评价和网络荟萃分析。骨关节炎软骨s1063 - 4584。
- Walrand S, Chiotelli E, Noirt F, Mwewa S, Lassel T(2008)食用含有胶原蛋白水解物的功能性发酵乳可提高血浆中胶原特异性氨基酸的浓度。农业食品化学56: 7790 - 7795。
- Bello AE, Oesser S(2006)胶原蛋白水解物治疗骨关节炎和其他关节疾病:文献综述。当前医学研究意见22日:2221 - 2232。(Crossref)
- Oesser S, Seifert J(2003)用降解胶原培养牛软骨细胞刺激II型胶原的生物合成和分泌。细胞组织311: 393 - 399。(Crossref)
- Schunck M, Schulze CH, Oesser S(2006)胶原水解物和葡萄糖胺对关节软骨细胞胞外基质代谢的不同功效。OA和软骨14: S114。
- Oesser S, Proksch E, Schunck M(2008)用一种特殊的水解胶原蛋白预防性治疗可减少膝关节软骨组织退变。OA和软骨16:S45。
- 李春华,李春华,李春华,李春华(2009)大鼠关节软骨组织中脯氨酸-羟脯氨酸的体外和体内保护作用。骨关节炎软骨17: 1620 - 1627。
- Clark KL, Sebastianelli W, Flechsenhar KR, Aukermann DF, Meza F等人(2008)24周的研究:将胶原蛋白水解物作为运动相关性关节疼痛运动员的膳食补充剂。当前医学研究意见24: 1485 - 1496。(Crossref)
- Zuckley L, Angelopoulou K, Carpenter MSS, Meredith BA等。(2004)水合胶原蛋白改善轻度膝关节炎患者的关节功能。体育运动医学与科学36: S153-S154。
- Moskowitz RW(2000)胶原蛋白水解物在骨关节疾病中的作用。半胱氨酸关节炎30: 87 - 99。(Crossref)
- bento - ruiz P, camaco - zambrano MM, Carrillo-Arcentales JN, Mestanza-Peralta MA, Vallejo-Flores CA等。(2009)食品成分胶原蛋白水解物改善关节舒适度的有效性和安全性的随机对照试验。[J]食品科学与营养60: 99 - 113
- Fitton JH(2011)褐藻糖聚糖的治疗;多功能海洋聚合物。3月的药物9: 1731 - 1760。(Crossref)
- 朴世宝,Chun KR, Kim JK, Suk K, Jung YM等。(2010)高分子量和低分子量岩藻胶蛋白对小鼠胶原诱导关节炎严重程度的差异影响。Phytother Res24: 1384 - 1391。(Crossref)
- Myers SP, O Connor J, Fitton JH, Brooks L, Rolfe M, Connellan P,等。(2010)海藻提取物营养复合物对骨关节炎影响的I期和II期联合开放标签研究。生物制剂4: 33-44。
- Kiple KF, Ornelas KC(2000)重要的蔬菜补充剂。见:Beck SV(编)《剑桥世界食物史》。剑桥大学出版社,英国剑桥1:231-249。
- Berteau O, Mulloy B(2003)硫酸盐岩藻多糖的新视角:硫酸盐岩藻多糖的结构、功能和生物学特性以及对该类多糖有活性的酶的概述。Glycobiolog13: 29-40。
- Myers SP, O 'Connor J, Fitton JH, Brooks L, Rolfe M,等。(2011)海藻提取物营养复合物免疫调节作用的一期和二期联合开放标签研究。生物制剂5: 45 - 60。
- Cunha TM, Verri WA Jr, Schivo IR, Napimoga MH, Parada CA等(2008)中性粒细胞在机械性炎症性高痛觉发展中的关键作用。[J]中华医学杂志83: 824 - 832。(Crossref)
- Lequesne MG(1997)髋关节和膝关节骨关节炎的算法功能指标。J Rheumatol24: 779 - 781。(Crossref)
- 李建平,李建平,李建平,等(2009)乳化鱼油对N -3脂肪酸的吸收。美国饮食协会109: 1076 - 1081。(Crossref)
- Felson DT,张勇(1998)膝关节和髋关节骨关节炎的流行病学进展及预防。关节炎感冒41: 1343 - 1355。(Crossref)
- Matheson AJ, Perry CM(2003)葡萄糖胺:在骨关节炎治疗中的应用综述。药物老化20: 1041 - 1060。(Crossref)
- 吴志强,吴志强,吴志强,吴志强(1998)口服硫酸软骨素对膝关节骨性关节炎进展的影响。骨关节炎软骨6(补充A): 39-46。





