背景:许多研究对COVID-19的死亡率和疾病严重程度预测因素进行了调查。然而,它们是基于来自高流行地区的早期或部分数据集。在此,我们回顾了低流行区已解决疫情的良性临床和流行病学结果相关因素。
方法:纳入2020年1月17日至2020年3月10日发生的一起地方性疫情中实验室确诊的98例新冠肺炎患者。数据更新,直到所有患者有最终结果。所有病人都住院了。
结果:病死率为1.0%。无局部继发感染病例。重症/危重率为19.4%。与重症/危重症患者相比,轻症/常见病患者入院时年龄小,无合并症,重要脏器功能及继发细菌感染指标正常。重症/危重症患者淋巴细胞计数在确诊前3天开始明显下降。发病第8天前无淋巴细胞减少,可排除78.5%的重症/危重症可能性。早期抗病毒治疗可显著缩短病毒rna阴性转化时间,其延迟与危重患者相关。
结论:所有患者尽早住院进行抗病毒治疗,防止二次流行是COVID-19重要的良性临床和流行病学结局相关因素。在低流行区采取积极的干预策略至关重要,而在高流行区,持续监测淋巴细胞可能有助于合理分类患者。
冠状病毒病-19 (COVID-19),临床转归、流行病学转归、临床特征、抗病毒治疗
冠状病毒病-2019 (COVID-19)已在全球确诊病例超过9990万人,病死率为3.0%[1]。COVID-19重症患者通常需要昂贵的重症监护,部分患者在忽视机械通气或体外膜氧合的情况下发展为成人呼吸窘迫综合征,死亡率高[2]。
文献对COVID-19的临床特征有很好的记载[3-5],有助于我们了解该病的流行病学、临床、实验室和影像学特征。一些研究对死亡率预测因子进行了关注[6-10]。年龄超过65岁、已有的潜在疾病、继发性细菌感染的存在和血液炎症指标的上升是致命结果的预测因素。此外,严重感染的患者更容易发生糖尿病、肾脏疾病和慢性肺部疾病,白细胞计数较高,淋巴细胞计数较低,c反应蛋白升高[11,12]。白细胞计数、丙氨酸转氨酶、天冬氨酸转氨酶、乳酸脱氢酶和降钙素原升高可预测重症监护病房入住[13]。然而,这些预测指标主要来自高流行地区,通常来自早期的部分流行数据集。所提出的模型确实被认为报告不足,存在高偏倚风险,其报告的表现可能是乐观的[6]。
新冠肺炎病死率随当地疫情强度的变化有显著差异。高流行省份为6.6%,而全国其他省份仅为0.8%(2020年1月25日更新),这表明高、低流行地区的死亡率和疾病严重程度预测指标可能存在显著差异。另一方面,疫情的解决或彻底解决,可能为减少高发区或新发区死亡人数和二次流行提供新的线索。基于上述原因,我们从已解决的98例病例(1例死亡,无局部继发感染)中进一步调查COVID-19的良性临床和流行病学结局相关因素。
研究设计和患者
这项单中心回顾性观察研究在中国广东省珠海市新冠肺炎定点医院中山大学第五附属医院进行。2020年1月17日至2020年3月10日,当地疫情中所有98名实验室确诊的COVID-19患者均住院治疗。
数据收集
从电子病历中提取所有患者的流行病学、人口统计学和临床数据、实验室检查结果、影像学报告和治疗方案。主要症状,实验室结果和入院时的胸部计算机断层扫描(CT)结果,最终的临床分类是根据整个病程进行的,除非另有说明。
实验室确认
中国疾病预防控制中心实验室确诊为严重急性呼吸综合征冠状病毒2型(SARS-CoV-2)感染。采用实时RT-PCR法检测鼻咽拭子标本中的SARS-CoV2 RNA[4]。
定义
根据中国国家卫生健康委员会发布的新冠肺炎诊疗指南[14],将患者临床分为轻度、常见、严重和危重型(标准见补充资料)。
治疗
大多数成年患者接受洛匹那韦和利托那韦的抗病毒治疗(分别为400mg每日两次和100mg每日两次,持续14天),阿比多尔(200mg每日三次,持续7-14天)和/或氯喹(500mg每日一次或两次,持续7天)。重症患者或48小时内肺炎进展超过50%的患者给予皮质类固醇(40-80 mg/天)和γ球蛋白(15-20 g/天)治疗3-5天。如果合并细菌或真菌感染,则给予喹诺酮类药物、大环内酯类药物或抗真菌药物。
当数据为正态分布时,连续变量以均数±标准差(SD)表示,采用学生t检验和Pearson相关分析进行比较。当数据为非正态分布时,变量表示为中位数(四分位间距,IQR),采用Mann-Whitney U检验和Spearman相关分析进行比较。分类变量以数字(%)表示,采用χ 2检验或Fisher精确检验进行比较。P<0.05认为有统计学意义。所有数据均采用SPSS(23.0版)软件进行分析。
临床和流行病学结果
本次本地疫情中所有98例实验室确诊的COVID-19患者均住院并纳入我们的分析。数据持续更新,直到所有患者获得最终临床结果(康复或死亡)。本次疫情的流行病学结果良好,没有卫生工作者和当地居民出现当地继发感染病例。这些患者包括5名儿童(14岁以下)和15名老年人(65岁以上),临床结果良好,病死率为1.0%(1/98)(表S1)。98例中,重症13例(13.3%),危重型6例(6.1%)。严重/危重率为19.4%(19/98)。6例危重患者(6.1%)均入住重症监护病房,其中3例(3.1%)接受了机械通气。只有一名78岁的高血压、冠心病和糖尿病患者死于成人呼吸窘迫综合征。发病至入院平均时间4.4天。平均住院时间为21.1天。 The mean period of the first viral RNA negative conversion was 8.2 days. The rate of re-positive viral RNA was 18.4%.
人口统计学和临床特征中的良性结局相关因素
98例COVID-19患者的人口学和流行病学特征见表S1。平均年龄46.3岁,男性45例(45.9%)。按疾病严重程度分层时,轻/普通病例的平均年龄(43.2岁)明显小于严重/危重病例(59.3岁)。P< 0.001)(表S1),提示较年轻的年龄是一个良性的临床结果相关因素。为了证实这一点,我们比较了4种不同临床类型的平均年龄以及不同年龄组中严重/危重病例的发生情况(图1)。病情越轻,平均年龄越年轻(图1A)。年龄组越年轻,重症患者比例越低(图1B)。合并症的自由似乎是另一个良性的临床结果相关因素(表S1)。然而,很明显,这种疾病的严重程度与高血压和糖尿病等与年龄有关的疾病有关。3例有呼吸道疾病史,其中2例有肺结核。发热、咳嗽和喉咙痛是最常见的三种症状,分别占57.1%、39.8%和9.2%(表S1)。
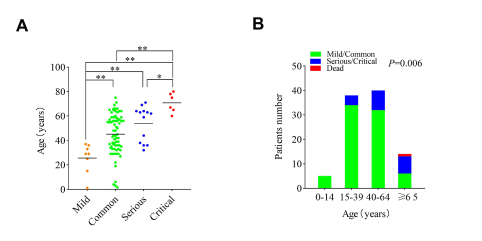
图1所示。不同临床类型COVID-19患者的平均年龄及年龄分布。(A)不同临床类型COVID-19患者的平均年龄。*P< 0.05, * *P< 0.01。(B) COVID-19患者年龄分布
实验室检查结果中的良性结果相关因素
入院时的实验室和胸部CT扫描结果见表S2。血常规检查显示,嗜酸性粒细胞、淋巴细胞和血小板计数下降与重症/危重症患者有显著相关性。淋巴细胞减少(< 1.0×109/L)在严重/危重病例中发生频率更高(图2A)。此外,重/危重患者淋巴细胞(图2B)、分化簇(CD3+)(图2C)、CD3+CD4+(图2D)和CD3+CD8+(图2E) T淋巴细胞和嗜酸性粒细胞(图2F)计数均显著降低。此外,将重/危重患者确诊日期前(发病平均7.8天)和轻/普通病例参照日期(发病平均第8天)的数据进行比较,我们发现,在确诊日期前3天,重/危重患者的淋巴细胞计数开始显著降低(图3)。对于轻/普通患者,其预测敏感性、预测特异性、发病第8天无淋巴细胞减少的阳性预测值为78.5%(62/79),阴性预测值为89.5%(17/19),96.9%(62/64),50.0%(17/34)。部分重症/危重症患者细菌感染指标c反应蛋白、降钙素原升高。此外,血清白蛋白的降低和血清g-球蛋白、总胆红素、乳酸脱氢酶、d -二聚体的升高与疾病严重程度显著相关(表S2),提示所有患者在出现明显呼吸困难、重要脏器发生实质性改变和继发细菌感染前入院是主要的良性结局相关因素。由于入院时间较早,除二氧化碳分压外,肺部相关结构功能指标、氧分压及胸部CT扫描结果在重症/危重症患者入院时变化不明显。
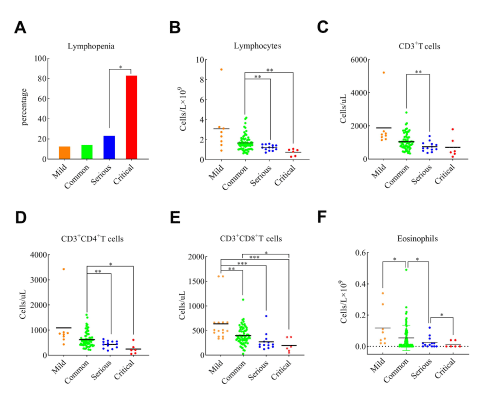
图2。不同类型COVID-19患者外周血淋巴细胞和嗜酸性粒细胞计数及淋巴细胞亚群。(A)不同临床类型COVID-19患者淋巴细胞减少发生率、(B)淋巴细胞计数、(C) CD3+T淋巴细胞计数、(D) CD3+CD4+T淋巴细胞计数、(E) CD3+CD8+T淋巴细胞计数、(F)嗜酸性粒细胞计数。*P< 0.05, * *P< 0.01
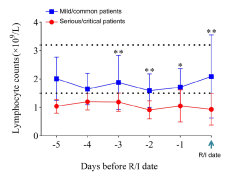
图3。新冠肺炎轻/普通、重/危重患者淋巴细胞计数早期动力学差异R/I日期,轻症/普通患者的参考日期/重症/危重症患者的鉴定日期。参照日期设定为第8天,相当于重/危重患者从发病确定的平均时间(7.8天)。分别分析轻度/普通(蓝线)和严重/危重(红线)COVID-19患者在R/I日期前不同时间点的淋巴细胞计数。误差柱,均值±SD。*P< 0.05, * *P< 0.01。上虚线为淋巴细胞计数正常上限,下虚线为正常下限
治疗中的良性结果相关因素
有关抗病毒药物、抗生素和皮质类固醇治疗的一般数据见表S1。氯喹、阿比多尔和洛匹那韦/利托那韦是当地流行的主要抗病毒药物。有些病人同时或依次使用两种或三种抗病毒药物。在不同临床类型中,抗病毒治疗率相似(图4A),但危重病例抗病毒治疗的平均延迟时间明显长于危重病例(图4B),这与病毒rna阴性转化时间较长(图4C)是一致的。抗病毒治疗对临床结局指标的影响见表1。发病后3天内开始抗病毒治疗可显著缩短病毒rna阴性转化时间。虽然没有统计学意义,但在接受抗病毒药物治疗的患者中,病毒RNA再阳性的比率相对较低。然而,抗病毒治疗的患者住院时间明显更长,这可能是由于各临床类型均倾向于对病情较重的患者给予抗病毒治疗。类似的趋势解释了抗生素和皮质类固醇延长了病毒rna阴性转化的时间或与更高的严重/临界率相关。因此,抗病毒治疗被确定为一个重要的良性临床结果相关因素。 Simultaneously, the treatments of antibiotics and corticosteroids might be also contributable to the benign clinical outcome of serious/critical cases due to the low case fatality rate (1.0%) in spite of the higher serious/critical rate (19.4%).
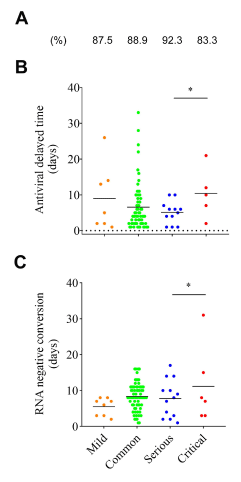
图4。抗病毒治疗与SARS-Cov-2 rna阴性转化时间。(A)不同临床类型COVID-19患者抗病毒治疗率、(B)抗病毒治疗延迟时间、(C) SARS-Cov-2 rna阴性转化时间。*P< 0.05
表1。治疗对临床结果的影响
数据以n(%)或平均值±标准差表示;重症、重/危重型患者;*P< 0.05, **P< 0.01,与下一行基准线比较。
尽管COVID-19演变为大流行,但缺乏标准化和令人信服的通用解决方案来阻止大流行或临床医生减少临床实践中的死亡人数。仔细回顾已解决的流行病,可能有助于找到一些有效的解决办法。珠海是中国的低流行区。当地疫情于1月初开始,到2020年3月底消失,最终病死率为1.0%,无本地继发感染病例。因此,该局部流行适合于良性临床和流行病学结局相关因素的分析。通过仔细回顾,我们发现年龄较小、无老年相关疾病、所有患者在发生明显呼吸困难前入院、重要器官发生实质性改变、继发细菌感染和早期抗病毒治疗是主要的良性临床和流行病学结局相关因素。在这些相关因素中,早期住院似乎是最重要的一个。它提供了早期抗病毒治疗、及时抗菌抗真菌治疗、合理护理和焦虑释放的机会。
基于死亡病例的COVID-19临床转归相关因素已被广泛研究[6-10]。致命的结果与65岁以上的年龄、先前存在的潜在疾病、继发感染的存在和血液炎症指标的上升有关。疾病严重程度与糖尿病、肾病、慢性肺部疾病等基础疾病以及白细胞计数增高、淋巴细胞计数偏低、c反应蛋白增高等异常相关[11,12]。基于本研究中解决的流行病,我们还发现年龄和潜在的合并症是与疾病严重程度相关的主要因素。此外,潜在的合并症主要是与年龄相关的疾病,如高血压和糖尿病。因此,年龄似乎是与疾病严重程度相关的关键因素。我们数据集的平均年龄为46.3岁,远低于中国(47-55岁)、意大利(65岁)、德国(65岁)和美国(65.5岁)[15-17]。仔细回顾中国某高疫区的报告,2020年1月16日至1月29日的平均年龄为42岁,2020年1月20日至2月14日的平均年龄为50-55岁[18,19],提示老年化是高疫区高病死率的重要因素。因此,确定年龄较轻是珠海市疫情发生的良性临床预后相关因素。
COVID-19最常见的实验室变化是淋巴细胞减少[4,20,21]。与轻/普通患者相比,本研究中重/危重患者淋巴细胞计数明显降低。重症/危重症患者淋巴细胞计数在确诊前3天开始明显下降。发病第8天前无淋巴细胞减少,可排除78.5%的重症/危重症可能性。这些发现有助于在高流行地区合理分类患者,减轻医疗系统的压力。除临床分型呼吸困难外,入院时的重/危重患者更容易出现其他重要器官功能异常、凝血及继发细菌感染[9,22-24]。这些异常在本研究中确实经常发生。然而,与高流行、高病死率地区的报道相比[4,18,25],我们患者入院时的总体症状(发烧、咳嗽)和实验室变化较轻,尤其是肺功能。我们的数据集从发病到入院的平均时间为4.4天,到诊断的平均时间为7.8天,这意味着大多数重/危重患者是在入院后被诊断出来的。事实上,包括死亡病例在内,只有2例患者在入院时出现呼吸困难。 In contrast, the average time for admission was 7.0 days in high epidemic and high case fatality rate area [25]. Therefore, laboratory data told us that early admission of all patients was the important benign clinical outcome-associated factor in this study.
虽然抗病毒药物在世界范围内都很受欢迎,但迄今为止还没有获得批准的抗病毒药物。然而,包括氯喹、阿比多尔、瑞德西韦和洛匹那韦/利托那韦在内的一些药物在降低死亡率方面已显示出令人鼓舞的效果[26-30]。在本研究中,大部分患者(88.8%)完成抗病毒治疗方案,且无明显副作用,且发病3天内开始早期抗病毒治疗可显著缩短病毒rna阴性转化时间,这与早期抗病毒治疗有助于减轻患者的严重程度和改善患者预后的观点一致[27],重型/危重型患者在标准护理之外使用洛皮那韦/利托那韦治疗未见获益[28]。危重病例抗病毒治疗的平均延迟时间明显长于重症病例,提示早期抗病毒治疗可能在防止重症向危重进展方面发挥作用,这可能与低病死率(1.0%)相关,尽管我们的数据集中严重/危重率较高(19.4%)。
由于大规模移民被认为促进了COVID-19在中国的早期传播,以及中国隔离患者和密切接触者的做法[31,32],所有患者的早期入院和广泛的抗病毒治疗可能有助于本次局部疫情的良性流行病学结果。早期入院和早期/广泛抗病毒治疗可能有助于预防社区和卫生工作者感染。然而,要控制新冠肺炎大流行,还存在许多不确定因素。同样,我们的成功经验在高流行地区是否有效也不确定,因为造成死亡的主要因素是缺乏足够的设施。然而,淋巴细胞的持续监测可能有助于通过合理分类患者来减轻医疗系统的压力。我们还强烈建议,在高流行地区,对适合当前大多数潜在抗病毒药物的轻症或年轻患者进行早期隔离和一般抗病毒治疗是必要的,以防止老年人或体弱者感染,减少死亡。
本研究得到广东省珠海市科技局2020年新冠肺炎专项资金支持。资金来源没有在收集、分析和解释数据方面发挥作用。
作者声明他们没有利益冲突。
本研究经中山大学第五附属医院伦理委员会批准。
查看补充数据
- 约翰霍普金斯大学(JHU)系统科学与工程中心(CSSE)的COVID-19仪表板。
- 杨欣,于燕,徐军,舒华,夏军,等。(2020)武汉市SARS-CoV-2肺炎危重患者临床病程及结局:单中心回顾性观察性研究。柳叶刀呼吸医学8: 475 - 481。
- 李魏Y,曾庆红W,黄X, J,邱X,李H, et al .(2020)的276名住院患者冠状病毒病的临床特点2019 Zengdu地区,湖北:单中心的描述性研究。BMC传染病20: 549。[Crossref]
- 关文杰,倪志勇,胡勇,梁文辉,欧长青,等。(2020)2019年中国冠状病毒病临床特征。[英]医学382: 1708 - 1720。
- 赵晓燕,徐晓霞,尹洪生,胡秋梅,熊涛,等。(2020)湖北省非武汉地区2019冠状病毒病患者临床特征的回顾性研究。BMC感染说20: 311。[Crossref]
- 李建军,李建军,李建军,等。(2020)新型冠状病毒感染诊断与预后预测模型的系统评价。BMJ69: m1328。[Crossref]
- 田伟,姜文,姚军,Nicholson CJ,李荣红等。(2020)新型冠状病毒肺炎住院患者死亡率的预测因素:系统评价和meta分析。医学病毒学92: 1875 - 1883。[Crossref]
- 阮强,杨凯,王伟,姜玲,宋杰(2020)基于武汉市150例新冠肺炎患者数据的临床预测因素分析。重症监护46: 846 - 848。[Crossref]
- 王峰,聂军,王辉,赵强,熊燕,等。(2020)COVID-19肺炎外周血淋巴细胞亚群改变特征。J传染病221: 1762 - 1769。[Crossref]
- 杜荣红,梁立荣,杨春青,王伟,曹振等。(2020)SARS-CoV-2感染的COVID-19肺炎患者死亡率预测因素的前瞻性队列研究。Eur呼吸器55岁:2000524。[Crossref]
- 王东,李锐,王军,姜强,高超,等。(2020)武汉市143例新冠肺炎患者病情严重程度与临床生化特征的相关性研究。BMC传染病20: 519。[Crossref]
- 季冬,张丹,徐军,陈志,杨涛,等。(2020)基于CALL评分的COVID-19肺炎患者进展风险预测。临床感染与疾病71: 1393 - 1399。[Crossref]
- 王晓明,王晓明,王晓明,等。(2020)新型冠状病毒肺炎临床预测模型的建立与验证。急诊医师实习生15: 1409 - 1414。[Crossref]
- http://www.nhc.gov.cn/yzygj/s7653p/202003/46c9294a7dfe4cef80dc7f5912eb1989.shtml
- 刘建军,刘建军,刘建军,等。(2020)中国新型冠状病毒病(COVID-19)的临床特征、实验室特征及预后分析。诊断(Berl)7: 91 - 96。[Crossref]
- (2020)意大利米兰地区新型冠状病毒肺炎临床结局的早期预测因子分析。中国Immunol217: 108509。[Crossref]
- Hoffmann C, Wolf E(2020)欧洲、美国和加拿大的老年群体和特定国家的COVID-19病死率。感染24: 1 - 6。[Crossref]
- 李锐,田静,杨峰,吕磊,于静,等。(2020)武汉市某三级医院225例新冠肺炎患者临床特征分析。临床病毒学127:104363。[Crossref]
- 张刚,胡超,罗丽,方芳,陈艳等。(2020)武汉市221例新型冠状病毒肺炎临床特征及短期预后分析。临床病毒学127: 104364。[Crossref]
- 刘健,李生,刘健,梁波,王霞等。(2020)SARS-CoV-2感染患者外周血淋巴细胞反应及细胞因子的纵向特征。EbioMedicine55岁:102763。[Crossref]
- 谭玲,王强,张丹,丁杰,黄强等。(2020)淋巴细胞减少对COVID-19疾病严重程度的预测研究。信号传导目标5: 33。[Crossref]
- Lippi G, Plebani M, Henry BM(2020)血小板减少与2019冠状病毒病(COVID-19)感染相关:一项荟萃分析。临床化学学报506: 145 - 148。[Crossref]
- 王峰,聂军,王辉,赵强,熊燕,等。(2020)COVID-19肺炎外周血淋巴细胞亚群改变特征。J传染病221: 1762 - 1769。[Crossref]
- 刘峰,徐安,张勇,宣伟,严涛,等。(2020)持续洛匹那韦联合用药可使COVID-19患者获益,嗜酸性粒细胞升高可预测COVID-19进展结局。国际传染病95: 183 - 191。[Crossref]
- 陈广文,黄文涛,唐仕伟(2020)2019冠状病毒病:流行病学、临床、防治证据和中西医结合治疗指南的最新进展。我是中医48: 737 - 762。[Crossref]
- 张建军,张建军,张建军,等。(2020)新型冠状病毒肺炎的临床研究进展。柳叶刀感染病20: 400 - 402。[Crossref]
- 吴健,李伟,石鑫,陈志,姜斌,等。(2020)早期抗病毒治疗有助于缓解新型冠状病毒病(COVID-19)患者的病情,改善预后。J实习医学288: 128 - 138。
- 曹斌,王勇,文迪,刘伟,王杰,等。(2020)洛匹那韦联合利托那韦治疗重症肺炎住院成人临床试验。[英]医学382: 1787 - 1799。[Crossref]
- 张建军,刘建军,刘建军,等。新型冠状病毒感染的临床研究[J] .武汉大学学报(自然科学版)。急诊医师实习生15: 841 - 843。[Crossref]
- Ferner RE, Aronson JK (2020) Remdesivir在covid-19中的作用。BMJ369: m1610。[Crossref]
- 宋文勇,臧鹏,丁志祥,方学勇,朱立荣等。(2020)大规模移民促进新冠肺炎在中国的早期传播:基于无标度网络的研究。感染贫困9: 109。
- [许立林,敖梅,周霞,朱文峰,聂海燕,等。(2020)人口大流动背景下中国防控新冠肺炎的实践。]感染贫困9: 115。[Crossref]





