本文综述了具有镇痛作用的选择性阿片受体激动剂RU-1205化合物对神经中介作用药物的影响。结果表明,大剂量(10和100 mg/kg) RU-1205可以预防安非他明诱导的小鼠过度运动,抑制左旋多巴和5- otp诱导的刻板印象,抑制微毒素诱导的癫痫发作,延长氟哌啶醇诱导的小鼠猝睡。用RU-1205化合物对小鼠进行预处理后,槟榔碱和尼古丁的作用与未进行预处理的小鼠相比没有变化。此外,利血平没有预防低运动和植物抑制作用。先前我们证实,1 mg/kg剂量的RU-1205可以抑制安非他明引起的运动过度和微毒素和二胡碱引起的癫痫发作,但当RU-1205与上述其他药物合用时没有变化。综上所述,RU-1205下kappa-opioid的激活与安非他明、L-DOPA、picrotoxin、利血平和5-OTP的作用存在剂量依赖性的功能相互作用。假设,所有这些都可能是kappa-opioid神经调节的结果。下一阶段的作用机制的确定,将是电生理测试使用膜片钳技术。但是,这些数据完全表明,在最佳镇痛剂量下,RU-1205不能强烈改变基本非痛觉神经传递分析仪的效果。
RU-1205,阿片受体激动剂,神经介质
缩写
or - kappa阿片受体,or - mu阿片受体,DOR-delta阿片受体,5- otp - 5-羟色胺,L- dopa - L-二羟苯丙氨酸
众所周知,阿片神经调节系统在中枢神经系统功能的调节中具有相当大的作用,包括高整合功能的调节,如记忆和学习、情绪和情绪控制的调节、动机、成瘾和厌恶、疼痛和敏感信号通路的调节、神经元超延伸性的控制和癫痫发作的预防[1]。因此,将kor模拟物和阻滞剂结合在一起,具有巨大的治疗潜力。新的镇痛化合物的创造是一个变种的药理学用途的KOR激活效应。与经典的阿片类镇痛药,如芬太尼或曲美培啶(promedol)相比,更少的滥用潜力和更少的镇痛耐受性是KOR激动剂的优势[1,2]。设计符合医疗标准的KOR镇痛药的一个步骤是研究新化合物与不同药物的相互作用(药物-药物相互作用临床前研究,AN Mironov编著的新医疗产品临床前研究俄罗斯总稿,2012)。这些行为的根本目的是回答“kappa-阿片样物质激活如何改变不同的神经介质系统?”这个问题。药物相互作用试验的另一个应用是研究潜在镇痛药临床管理的特殊性,因为药物相互作用问题严重,特别是中枢活性药物。
本文介绍了一种新型强效镇痛药和kor激动剂RU-1205(1、10和100 mg/kg)对安非他明、左旋多巴、5-羟色胺、微毒素、氟哌啶醇、茴香碱和尼古丁等药物行为效应的影响。延续了我们之前的研究结果,1 mg/kg的RU-1205可以抑制安非他明的作用,降低GABA阻滞剂如微毒素和二胡碱的癫痫致尿潜能[3]。
有不同类型的神经中介,包括传入信号的转换和处理以及相关的行为,心理活动,运动和其他行为。神经介质如5-羟色胺、多巴胺、组胺、谷氨酸、GABA等参与并被KOR调节。除了阿片类镇痛药外,潜在的KOR激动剂使用临床管理的有趣领域是成瘾和戒断的治疗。当使用精神药物时,KOR激活会抑制戒断性NMDA过度激活(蓝斑)和腹侧被盖区多巴胺释放[1,4,5]。此外,在治疗神经退行性疾病,如帕金森病或运动神经元疾病(MND)方面,KOR激活也有潜在的应用前景。KOR激活可以阻止nmda介导的运动神经元去极化,抑制l - dopa诱导的运动障碍,在单胺消耗诱导的帕金森病(利血平诱发)时刺激运动[6,7]。在手术前用药的情况下,可以使用麻醉和抗精神病药物(氟哌啶醇)的组合。许多这些情况需要使用不同的药物产品与神经调节或神经调解活动。因此,在任何相应的大脑区域,KOR的激活都可以释放或增强特定神经介质修饰产物的作用。
RU-1205化合物在大剂量范围内(0.001-100 mg/kg, ED50 0.02 mg/kg,热板,小鼠)和不同类型的伤害感觉模型(CNS伤害感觉模型,如热板和甩尾,以及神经性、炎症性和内脏性疼痛模型)具有镇痛活性,这在之前的研究中得到了证实[8]。该化合物的镇痛活性是由KOR激活介导的。此外,RU-1205化合物在体外(离体组织电致收缩模型)不激活mu-和delta-阿片受体,在体内不具有MOR和DOR激活的典型特异性不良反应,如呼吸抑制、肠道运动障碍、镇静或愉悦行为。最后,RU-1205具有非典型的kor相关不良反应[8-10]。
研究对象:RU-1205化合物(块状,来自俄罗斯罗斯托顿南联邦物理与有机化学大学);实验动物:异交成熟小白鼠20-25 g,昼夜节律倒转。实验程序从上午11点到下午16点进行。试验前处理动物3周。所有实验均按照欧洲议会和欧盟理事会关于保护用于科学目的的动物的指令2010/63/EU(2010年9月22日)的要求进行。所有麻醉药品实验均在LO-34-04-000022(12.10.2012)许可下进行,用于麻醉药品、精神药物和前体的工作和传播控制。
所有溶液均在蒸馏水上配制并腹腔注射。RU-1205化合物在联合用药前60分钟注射。时间是根据化合物的药代动力学性质来选择的。重新收集了1 mg/kg剂量RU-1205的所有影响数据,并与先前发表的数据进行了比较[3]。我们给出了早期的结果,因为它需要更完整的数据表示。每组8只(n=8)。
神经介质分析仪的调节效应
我们研究了被试化合物与神经递质分析仪对多巴胺能、去甲肾上腺素能、胆碱能和氨基丁酸能系统的典型影响的相互作用。在Mironov博士编著的《新药临床前研究总稿》(rus号稿件)中描述了行为测试。通过运动变化(Ugo Basile)评估安非他明和利血平对疗效的影响;氟哌啶醇作用的影响——通过麻痹持续时间的变化(强迫“讲师”姿势的持续时间);运动剧烈程度对左旋多巴作用的影响;槟榔碱和尼古丁对癫痫发作潜伏期的影响;5-OTP -对刻板印象持续时间的影响。
Amphetamine-indiced hyperlocomotion
将动物分为5组。各组治疗方案见表1。
表1。安非他明引起的过度运动方案。
不。组 |
ru - 1205 /剂量 (安非他明前60分钟) |
安非他命 (测试前30分钟) |
1(阴性对照) |
——(汽车) |
——(汽车) |
2(阳性对照) |
——(汽车) |
+ |
3(最佳剂量组) |
+ / - 1毫克/公斤 |
+ |
4(中高剂量组) |
+ / 10毫克/公斤 |
+ |
5(高剂量组) |
+ / 100毫克/公斤 |
+ |
本试验分为阳性对照组和阴性对照组。阳性对照动物ig安非他明6 mg/kg,阴性对照动物ig载药。定量测量运动活动时采用Ugo Basile动作计。每只动物被单独放置在测乳仪的盒子里,以显示其完全运动。测量时间为5分钟。
L-DOPA-induced机械重复
将动物分为8组。各组治疗方案见表2。
表2。左旋多巴诱导刻板印象方案。
不。组 |
ru - 1205 /剂量 (左旋多巴前60分钟) |
左旋多巴200mg /kg (测试前30分钟) |
左旋多巴500mg /kg (测试前30分钟) |
1(低剂量控制) |
——(汽车) |
+ |
- - - - - - |
2(高剂量控制) |
——(汽车) |
- - - - - - |
+ |
3(最佳剂量组) |
+ / - 1毫克/公斤 |
+ |
- - - - - - |
4(中高剂量组) |
+ / 10毫克/公斤 |
+ |
- - - - - - |
5(高剂量组) |
+ / 100毫克/公斤 |
+ |
- - - - - - |
6(最佳剂量组) |
+ / - 1毫克/公斤 |
- - - - - - |
+ |
7(中高剂量组) |
+ / 10毫克/公斤 |
- - - - - - |
+ |
8(高剂量组) |
+ / 100毫克/公斤 |
- - - - - - |
+ |
在这个测试中有两个对照组。阳性对照组给予500 mg/kg左旋多巴处理。该剂量可引起运动障碍和刻板反应(眩晕、直立)。阴性对照组给予200 mg/kg左旋多巴。对于任何特定的可见反应,剂量都太小了。实验组,先前注射RU-1205,低剂量或高剂量左旋多巴处理。解释结果的半定量量表:1分-罕见异常运动小于50%的观察时间;2分-频繁异常动作占观察时间的50%;3分-连续异常运动行为,对听觉刺激反应正常; 4 scores - continuous abnormal motor acts without reaction to the auditory stimulus.
氟哌啶醇的镇痛作用
强迫的“讲师式”姿势对老鼠来说是不舒服的姿势。健康的非过敏动物试着离开这个姿势。对照组在试验前20分钟ig氟哌啶醇1 mg/kg。实验组在氟哌啶醇注射前60分钟分别给予RU-1205 1、10或100 mg/kg。将小鼠前腿放置在高架平台上,如果发展为麻痹,则不动。截止时间为3分钟。当发生猝厥时,纹状体中多巴胺信号传导失败,多巴胺/5-羟色胺相互作用失衡[11]。
5-OTP-induced机械重复
对照组和试验组均给予5-OTP 300 mg/kg ig, 10 min后开始登记。如上所述,在5-OTP注射前60分钟给非对照动物注射3种不同剂量的RU-1205(1、10或100 mg/kg)。在5-OTP注射后10分钟、20分钟和30分钟时间点计算1分钟内头抽搐次数。头抽搐反应是一种快速的左右旋转头部运动。5-OTP诱导5-HT尖峰,5-HT2A受体在额叶(前额皮质)的激活是代谢性谷氨酸受体激活和头部运动形成的原因[12]。
利血平的神经抑制作用
利血平是本研究中使用的最非选择性的单胺类药物。这种药物导致大脑中单胺(去甲肾上腺素能、5-羟色胺能、多巴胺能)的非选择性消耗。但众所周知的事实是,激活KOR具有减少利血平引起的低运动的效力[13]。研究RU-1205对利血平所致低运动、上睑下垂和低体温的影响。剂量为利血平2.5 mg/kg。我们使用的测试方案见表3。
表3。利血平治疗和时间点方案。
不。组 |
时间点1 (利血平注射) |
时间点2 (4小时后, 注射RU-1205) |
时间点3 (30分钟后 ru - 1205注射) |
1(阴性对照) |
——(汽车) |
——(汽车) |
所有测量 |
2(阳性对照) |
+ |
——(汽车) |
3 RU-1205 1mg/kg |
+ |
+ |
4 RU-1205 10mg/kg |
+ |
+ |
5 RU-1205 100mg/kg |
+ |
+ |
槟榔碱引起的震颤和运动障碍
如果以背纹状体区(尾状核)为靶点,中枢神经系统中-胆碱激活可产生刻板行为和运动障碍反应,如震颤。对照组和试验组分别给予槟榔碱25 mg/kg ig,在注射槟榔碱前60分钟分别给予3种不同剂量的RU-1205(1、10、100 mg/kg)。
尼古丁引起的癫痫反应
尼古丁受体参与心理和运动调节。当受体被阻断或激活时,尼古丁引起的运动协调障碍、震颤和癫痫发作的潜伏期分别变长或变短。剂量为6 mg/kg, s.c.。动物分为3个试验组和1个对照组。各组在给药前60分钟分别给予不同剂量的RU-1205(1、10、100 mg/kg)或对照药后注射尼古丁,并立即开始记录震颤和癫痫发作潜伏期。震颤和癫痫发作的发展是一个快速的过程。
微毒素致痫性尿源作用
Picrotoxin是一种变构gabaa受体阻滞剂,可诱发癫痫样活动和癫痫发作。微毒素的剂量为10 mg/kg s.c。测定震颤潜伏期、癫痫发作和死亡时间。
采用Kruscal-Walles检验(Dunns后验,<0.05),ANOVA (Tukey后验,p<0.05)进行统计学分析。在选择统计标准时,我们使用Kolmogorov-Smirnov检验来估计正态性,如果是正态,我们使用方差分析,如果不是,我们使用KruscalWalles检验。在所有情况下,作为平均值标准误差(SEM)提交的平均值的分布。
早期我们报道了1 mg/kg RU-1205对安非他明、氟哌啶醇、左旋多巴、槟榔碱、尼古丁、5-OTP、利血平和微毒素作用的影响[3]。1 mg/kg为RU-1205不同伤害性试验的平均最大有效剂量。
RU-1205对上述药物作用影响的完整信息见表4。detalisation。
表4。RU-1205化合物对体内神经介质分析仪作用的影响。
RU-1205剂量,mg/kg 的影响 |
1 |
10 |
One hundred. |
胆碱能系统 |
槟榔碱引起的震颤,强度,持续时间 |
没有变化 |
没有变化 |
没有变化 |
尼古丁引起的震颤,癫痫 |
没有变化 |
没有变化 |
没有变化 |
GABA-ergic系统 |
picrotoxin诱发震颤,癫痫 |
抑制 |
抑制 |
强烈的抑制 |
5-HT-ergic系统 |
5-OTP-induced运动过度 |
没有变化 |
抑制 |
强烈的抑制 |
单胺能系统(主要神经递质) |
安非他明引起的过度运动(多巴胺) |
抑制 |
抑制 |
强烈的抑制 |
氟哌啶醇诱导的催化作用(多巴胺) |
没有变化 |
没有变化 |
强烈的抑制 |
左旋多巴诱导的运动亢进(多巴胺) |
没有变化 |
抑制 |
强烈的抑制 |
利血平诱导的低运动(多巴胺) |
不能消除 |
不能消除 |
不能消除 |
利血平所致体温过低,上睑下垂(混合性) |
没有变化 |
没有变化 |
强烈的抑制 |
安非他明对过度运动效应的影响
阳性对照组平均自发运动量是阴性对照组的2倍。RU-1205抑制安非他明的过度运动效应呈剂量依赖性(表5)。
表5所示。RU-1205对安非他明过度运动效应的影响。注* -与阴性对照比较显著;# -与阳性(仅安非他明治疗)对照相比显著(Kruskal-Wallis单向方差分析,Dunn后验,p < 0.05)。
不。组 |
运动活动(M±SEM) |
1(阴性对照) |
133年,1±12、3 |
2(控制) |
265,2±13,7* |
3 (1 mg/kg剂量组) |
240年,35 0±3 * |
4 (10 mg/kg剂量组) |
120,8±13,1# |
5 (100 mg/kg剂量组) |
53,7±9,0# |
1 mg/kg RU-1205诱导过度运动减少约为仅安非他明处理组的40%。10 mg/kg RU-1205和100 mg/kg RU-1205预处理小鼠的过度运动压迫分别比阳性对照组减少65%和80%。
对左旋多巴刻板印象的影响
低剂量对照组未出现任何异常行为症状。相比之下,高剂量左旋多巴引起严重的运动障碍和高多巴胺相关行为(表6)。
表6所示。RU-1205对左旋多巴运动障碍效应的影响(评分,M±SEM)。注* -与低剂量对照相比显著;# -与高剂量对照组比较显著(方差分析,Tukey后检验,p < 0.05)。
不。组 |
不正常的动作 低剂量的左旋多巴 |
不正常的动作 高剂量的左旋多巴 |
1(低剂量控制) |
0.4±0.1 |
- - - - - - |
2(高剂量控制) |
- - - - - - |
4.0±0.0* |
3 (RU-1205 1mg /kg) |
0.3±0.2 |
3.2±0.1* |
4 (RU-1205 10 mgkg) |
0.0±0.0 |
1.1±0.2# |
5 (RU-1205 100mg /kg) |
0.0±0.0 |
0.3±0.2# |
因此,RU-1205对左旋多巴动力障碍有较强的抑制作用,无增强作用。
氟哌啶醇对镇痛作用的影响
氟哌啶醇对照组小鼠离开强迫姿势的平均潜伏期为93.7±15.7秒。早期我们确定RU-1205 1 mg/kg不能改变氟哌啶醇诱导的猝厥。10 mg/kg的剂量也没有显著影响,但有生长的趋势,但没有显著性。RU-1205的最大剂量(100 mg/kg)可使昏迷时间明显延长(表7)。
表7所示。RU-1205对氟哌啶醇催化作用的影响(M±SEM)。注:* -与对照比较显著(Kruskal-Wallis单因素方差分析,Dunn后验,p < 0.05)。
不。组 |
持续时间目录,秒 |
1(对照组) |
93.7±15.7 |
2 (RU-1205 1mg /kg) |
89.8±12.7 |
3 (RU-1205 10mg /kg) |
117.4±8.6 |
4 (RU-1205 100mg /kg) |
180.0±0.0* |
对5-OTP效果的影响
5-OTP剂量为300 mg/kg的对照动物出现头抽搐。与对照组相比,RU-1205 1 mg/kg组未出现抽搐次数。10 mg/kg和100 mg/kg的RU-1205对抽动的减少幅度太大(图1)。
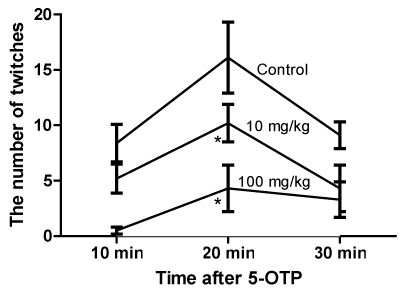
图1所示。RU-1205对5- otp诱导的头抽搐的影响(M±SEM)。注:*-与对照组比较显著(方差分析,检验后方差分析,p<0.05)。为了更清楚,图上没有显示1mg /kg RU-1205的剂量。
利血平对神经抑制作用的影响
在对照组动物(仅利血平治疗)中,出现运动能力低下(与未治疗的动物相比,96.2%的运动受到抑制),直肠低温(平均体温下降约2.2°С)和上睑下垂(平均眼间隙约1.4±0.6 mm)。详细情况见表8和表9。
表8所示。RU-1205对利血平降血压作用的影响(M±SEM)。注:*-与阴性对照比较显著;与利血平治疗组比较,差异有统计学意义(方差分析,检验后方差分析,p < 0.05)。
不。RU-1205组/剂量 |
运动 |
1(阴性对照) |
133.1±2.3 |
2例(仅利血平治疗对照) |
5.1±0.7* |
3 (RU-1205 1mg /kg) |
3.7±1.2* |
4 (RU-1205 10mg /kg) |
30.1±0.5*# |
5 (RU-1205 100mg /kg) |
1.2±0.8* |
表9所示。RU-1205化合物对利血平致低温和上睑下垂的影响(M±SEM)。
不。组 |
温度 |
上睑下垂 |
在利血平 |
4小时后, RU-1205注射时间点 |
RU-1205注射后30分钟 |
在利血平 |
4小时后, RU-1205注射时间点 |
RU-1205注射后30分钟 |
1(阴性对照) |
37.8±0.3(车) |
37.5±0.5(车) |
37.3±0.3(车辆) |
3.0±0.0 (车辆) |
3.0±0.0(车辆) |
3.0±0.0(车辆) |
2例(仅利血平治疗) |
38.2±0.4 |
35.5±0.5*(车辆) |
35.3±0.7(车辆) |
3.0±0.0 |
1.2±0.4*(车辆) |
1.4±0.6*(车辆) |
3 (1mg /kg) |
38.4±0.3 |
35.5±0.5* |
35.4±0.9* |
3.0±0.0 |
1.1±0.4* |
1.5±0.5* |
4 (10mg /kg) |
38.4±0.3 |
35.5±0.7* |
35.0±1.4* |
3.0±0.0 |
0.5±0.1* |
0.8±0.2* |
5 (100mg /kg) |
38.0±0.5 |
34.5±0.5* |
32.1±0.2* # |
3.0±0.0 |
0.6±0.2* |
0.0±0.0版权所有OAT。版权所有 |
1、10或100 mg/kg RU-1205与2.5 mg/kg利血平和单独2.5 mg/kg利血平联合治疗组之间的运动无显著差异。经测定,利血平单药组与ru - 12051 1和10 mg/kg治疗组直肠温度无显著差异。100mg /kg RU-1205治疗组对直肠温度有较深的抑制作用(与利血平相比下降9.1%)。
对槟榔碱效果的影响
仅用槟榔碱治疗的对照组发生震颤,潜伏期67.3±9.0秒,持续时间1107.0±59.6秒。RU-1205没有改变槟榔碱的作用(数据未提供,Kruscal-Wallis检验,Dunn后验)。
与尼古丁的相互作用
在只服用尼古丁的动物中,震颤的平均潜伏期为61.0±5.1秒,癫痫发作的平均潜伏期为100.5±4.4秒。对照组与RU-1205预处理组之间无显著差异(数据未提供,采用Kruscal-Wallis检验,Dunn’s后验)。
对微毒素作用的影响
对照组震颤潜伏期为253.3±41.5秒,发作潜伏期为368.2±56.3秒。平均发作次数24.0±4.2次。我们只计算了伴有身体翻转的强直阵挛性发作。注射微毒素后死亡的平均时间为860.0±90.2秒。RU-1205化合物在剂量为1 mg/kg时无显著影响,但在剂量为10 mg/kg时(震颤潜伏期延长40%)和100 mg/kg时(所有标记条件下预防时间延长,震颤潜伏期延长2.5倍,发作潜伏期延长6倍,发作次数延长6.4倍,死亡时间延长2.4倍)均有显著影响(Kruskal-Wallis检验,Dunns后验检验,p<0.05)。
在KOR激动剂RU-1205化合物下的KOR激活效果与经典的KOR激动剂(如U-50,488H或U-62,066E(螺旋喹啉))相似。当KOR被激活时,背侧、腹侧纹状体区和腹侧被盖区(VTA)的多巴胺水平下降。我们观察到高剂量左旋多巴引起的行为破坏,通常与左旋多巴、卡麦角林等引起的多巴胺超载有关[14]。此外,左旋多巴引起的运动障碍的有效医疗管理仍然是帕金森病患者未满足的需求[4,5]。没有数据表明,在健康受试者中,KOR激活和随后的多巴胺抑制是医源性帕金森病的病因(然而,在灵长类动物SN变性实验模型中,当左旋多巴诱导运动障碍时,KOR激活会使帕金森病恶化并伴有运动障碍减少)[7]。基底节区阿片传递的改变提示了多巴胺模拟运动障碍的治疗机会。因此,我们确定RU-1205预处理可以预防左旋多巴诱导的刻板印象和运动障碍。有典型的KOR激活效应。此外,只有在10mg /kg及以上时才观察到足够强的运动障碍抑制效果,而在我们之前的研究中,1mg /kg时没有观察到。以前我们报道过10mg /kg的RU-1205不是危险剂量(1mg /kg是最大镇痛剂量)。 Only mild hypothermia and no any other adverse reactions are developed when 10 mg/kg i.p. [10]. So, the potential usage of the compound in different doses may have different appointments. This is an interesting remark.
背纹状体区和黑质是运动协调器。纹状体腹侧部分在情绪和动机的调节中起作用。这个区域也受到KOR神经调节的调节。这是奖励系统的一部分。KOR激活会导致VTA和腹侧纹状体多巴胺丢失[4,5]。中边缘和中皮质通路是VTA的两个主要输出:它们都是多巴胺能和kor调节的。这两种途径都被安非他明急性治疗激活。在1、10和100 mg/kg RU-1205组中,安非他明引起的过度运动的减少程度分别比仅安非他明组低40%、65%和80%。在10 mg/kg的情况下,自发运动的绝对水平在负控制值附近。在100 mg/kg RU-1205的情况下,平均运动的绝对值比阴性对照组小2.5倍。 In results, we determined that kappa-opioid agonist RU-1205 can oppress the locomotor effect of amphetamine. This is associated with contraversion of dopamine levelup in the mesolymbic pathway when KOR is activated. There is a typical effect of KOR activation too.
下一个固有的能力,KOR激动剂是增强氟哌啶醇诱导的麻痹。基本上,阿片类药物和抗精神病药物相互增强作用。当两种产品联合使用时,可能会观察到镇痛时间延长和氟哌啶醇超载的风险。在10mg /kg时表现出增强猝睡持续时间的趋势,而在100mg /kg时表现出较强的显著性。猝倒是纹状体多巴胺丢失和5-羟色胺失衡的结果。还有第三种典型的KOR激活效应。有趣的是,在0.1 ~ 100 mg/kg剂量下,RU-1205不能诱导自身的催化作用。
基于这三个测试,我们可以得出结论,RU-1205对运动纹状体(壳核、尾状核)的KOR激活的影响远低于纹状体腹侧部分(伏隔核)和VTA。
利血平与RU-1205联合给药达到预期效果。低血压部分排出。这与预期的KOR激动剂一致。激活KOR可以减少利血平引起的低运动[13]。我们确定1mg /kg的RU-1205无效。这与我们以前的结果有关。10 mg/kg剂量有效,降低利血平的低运动作用。其次,最高剂量下的镇静作用可能是RU-1205刺激运动的钟形剂量反应曲线的基础。先前我们确定,运动减退可能是RU-1205自身的影响,但剂量高于最大镇痛药1mg /kg (20mg /kg或更多)。在本研究中,RU-1205的运动刺激作用可能部分是由于对基底神经节输出区域的影响。 However, activation of KOR in the striatum inhibits the release of glutamate from striatal nerve terminals. Additionally, the activation of locomotion by RU-1205 might also be due to an effect on glutamate transmission in the striatum (inputs from the front lobes). Reserpine depress basic monoaminergic transmittions (dopamine, 5-HT, noradrenalin) and can reduce the body temperature. We determined that there were no significant differences between rectal temperature of animals, treated with reserpine only and combined with RU-1205 1 mg/kg or 10 mg/kg. But there was a loss of body temperature 9.1% in comparison with reserpine treated only when dose 100 mg/kg was used. This was expected [15]. The hypothermic results and assumptions about its mechanistic are described in our previous paper [10].
5-OTP是下一个单胺分析仪和5-HT的直接前体。本文研究了RU-1205激活对5- otp诱导的抽搐的抑制作用。抽搐的机制很复杂。这种刻板印象形成的主要作用是前叶中的5- ht -谷氨酸相互作用[16,17]。不仅5-OTP可以诱导这种活性,而且这种反应还需要代谢谷氨酸受体的激活。KOR神经调节的概念表明,激活KOR可以通过抑制谷氨酸释放来抑制谷氨酸能突触后增强。神经调节的KOR机制包括在许多区域抑制5-HT的释放,如中缝核和抑制前额皮质的谷氨酸。因此,在这种情况下,无法总结RU-1205(谷氨酸能、5- ht能或两者兼有)的假设作用机制。但有一个有趣的问题:1)头抽搐是对5-羟色胺刺激物的致幻剂特异性反应;2)在某些情况下,KOR激活可产生自身的精神病效应; 3) is KOR activation can prevent 5-HT-induced psychosis induced by some narcotics such as LSD? This assumption of KOR activation usage is in opposition to the main clinical observations that KOR activation induces own hallucinogenic reaction. So, the suppression of head-twitches formation and hallucinogenic action simultaneously – there is a new challenge for KOR investigators [18].
我们使用的下一个分析仪是胆碱能物质尼古丁和槟榔碱。钌-1205对该分析仪的检测效果没有影响。给小鼠注射毒蕈碱胆碱受体激动剂槟榔碱可引起持久震颤。槟榔碱震颤的发病机制主要与nmda受体有关。适度阻断ampa型受体可以增强混合作用拮抗剂(抗nmda +抗ampa)的预防作用,尽管对ampa型受体的阻断作用的优势阻止了这种作用[19]。前文我们讨论了kor介导的谷氨酸神经兴奋性的预防。但本研究结果表明,KOR活化对槟榔碱的作用没有影响。为什么?有假设认为,KOR参与谷氨酸诱导的反应调节独立于间胆碱能反应。最后,研究表明激活KOR可以预防匹罗卡品引起的震颤和癫痫发作,但在目前的研究中没有观察到RU-1205具有相同的抗胆碱能活性[18]。 The same situation is developed around influence of RU-1205 on the acute nicotine-induced tremor. The last finding suggests that nicotine-induced tremor’s mechanism of development involves 5-HT neuromediation [20]. There are 5-HT1A and 5-HT2A receptors can to potentiate and attenuate this tremor respectively, if activated by selective agonists. The reduction of 5-OTP twitches, observed previously, is in opposition with our current findings. Current findings suggest that there are different mechanisms of regulation of 5-HT release in KOR-associated suppression of head-twitches and nicotine-induced tremoris. So, KOR regulation is not involved or involved otherwise in the nicotine-induced tremor than in 5-OTP-induced stereotypy despite both reactions are 5-HT-dependent ultimately.
最后一种分析仪是微毒素。在单一治疗和点燃模型中,KOR激活剂的典型作用是减少GABAA阻滞剂引起的癫痫发作[21]。电生理、生化和药理学数据支持强啡与特定类型癫痫发作有关的假设。有明确的证据表明,对于复杂的部分(边缘)癫痫,即。颞叶癫痫的那些特征,因为;(1) dynorphin在边缘系统的各个部位高度表达,特别是在海马的颗粒细胞中;(2)在复杂的部分性癫痫发作时,海马体(和其他脑区)似乎释放了肌啡;(3)释放的肌啡抑制海马多突触的兴奋性神经传递通过阿片受体的活化;(4) kappa阿片受体激动剂对边缘癫痫发作非常有效。关于全身性强直-阵挛性发作的数据则不那么直接。Picrotoxin是一种致痫性尿源化合物,其作用是通过包括大脑边缘系统在内的多个系统实现的。此外,黑质KOR系统在激活抗癫痫系统和限制picrotoxin诱导的癫痫发作中起着重要作用[22]。
总之,我们确定了新型kappa-阿片化合物对神经介质分析仪(激活剂和阻滞剂)作用的影响。我们检测到RU-1205下kappa-阿片样物质的激活与安非他明、左旋多巴、微毒素、利血平和5-OTP的作用呈剂量依赖性的功能相互作用。假设,所有这些都可能是kappa-opioid神经调节的结果。下一阶段的作用机制的确定,将是电生理测试使用膜片钳技术。但是,这些数据完全表明,在最佳镇痛剂量下,RU-1205不能强烈改变基本非痛觉神经传递分析仪的效果。
通讯作者(Litvinov博士)感谢Daria D. Shamshina (VolSMU,伏尔加格勒,俄罗斯)在编写文本和进行实验时给予的灵感和支持。
- 帕斯捷尔纳克GW(2011)阿片受体。NJ:人类出版社,第497页。
- Chavkin C(2011)阿片类药物治疗疼痛和成瘾的治疗潜力。神经精神药理学36: 369 - 370。
- Spasov AA, Grechko OY, Shtareva DM, Rashchenko AI (2014) RU-1205与神经递质分析仪的相互作用研究。J Volg SMU: 120 - 122。
- Cahill CM, Taylor AMW, Cook C, Ong E, Morón J A等。(2014)kappa阿片受体系统是否有助于疼痛厌恶。前药物杂志5: 253。
- Land BB, Bruchas MR, Schattauer S, Giardino WJ, Aita M,等。(2009)中脑背核kappa阿片受体的激活介导应激的不良反应和恢复药物寻求。美国国家科学基金委106: 19168 - 19173。(Crossref)
- (2015)阿片受体双κ-激动剂/μ-拮抗剂调节左旋多巴诱导的运动障碍和纠正纹状体异常变化的非人灵长类动物模型。安神经77: 930 - 941。
- Cox H, Togasaki DM, Chen L, Langston JW, Di Monte DA等。(2007)选择性kappa-阿片受体激动剂U50,488在mptp治疗的灵长类动物中减少左旋多巴诱导的运动障碍,但恶化帕金森病。实验神经205: 101 - 107。
- Grechko OY, Litvinov RA, Spasov AA, Rashchenko AI等。(2017)不同κ-受体选择性制剂中μ-和δ-阿片活性的研究。公牛Exp生物医学162: 632 - 635。(Crossref)
- 葛丽娟,李丽娟,李丽娟,等(2016)苯并咪唑衍生物对炎症性疼痛模型的镇痛作用。J Volg SMU58: 101 - 103。
- Spasov AA, Grechko OY, Eliseeva NV, Litvinov RA, Shamshina DD (2017) kappa -阿片激动剂Ru-1205化合物对野生型小鼠神经功能的毒性作用。J克林制药3: 1014。
- Reavill C, Kettle A, Holland V, Riley G, Blackburn TP (1999) 5-HT2C受体拮抗剂对氟哌啶醇诱导的猝厥的抑制作用。医学杂志126: 572 - 574。
- Moreno JL, Holloway T, Albizu L, Sealfon SC, González-Maeso J(2011)代谢性谷氨酸mGlu2受体在致幻5-HT2A受体激动剂诱导的药理学和行为学效应中的作用。>列托人493: 76 - 79。
- Hill MP, Brotchie JM(1999)肾上腺素能受体激动剂,可定,增强选择性卡帕-阿片受体激动剂,依纳多啉在单胺衰竭大鼠中的抗帕金森作用。医学杂志128: 1577 - 1585。
- encaracion EV, Hauser RA(2008)左旋多巴诱导的帕金森病运动障碍:病因学、对生活质量的影响和治疗。欧元神经60: 57 - 66。(Crossref)
- Baker AK, Meert TF(2002)全身给药阿片受体亚型激动剂和拮抗剂对小鼠体温的功能影响。[J]药物与实验302: 1253 - 1264。(Crossref)
- [González-Maeso]王荣,袁涛,陈平,等。(2008)血清素/谷氨酸受体复合物在精神病中的作用。自然452: 93 - 97。
- Tao R ., Auerbach SB .(2002)阿片受体亚型对大鼠中枢神经系统血清素外排的差异调节。[J]药物与实验303: 549 - 556。
- 黄春华,李春华,李春华,等(1994)阿片受体激动剂对匹罗卡平致癫痫的抑制作用。欧元Neuropsychopharmacol4: 527 - 533。
- Lukomskaya NY, Lavrent'eva VV, Starshinova LA, Zhabko EP, Gmiro VE等。(2008)嗜离子性谷氨酸受体参与小鼠胆碱性震颤的发生。神经科学行为物理38: 421 - 426。
- 李春华,李春华,李春华,等。(2017)尼古丁诱导小鼠震颤的血清素能调节。J药物科学134: 131 - 138。(Crossref)
- Kryzhanovskii GN, Shandra AA, Godlevskii LS, Mazarati AM, Nguyen TT(1991)海马和黑质在微毒素诱发的行为和惊厥障碍中的作用。俄文文章。Biull Eksp生物医学111: 235 - 239。
- M ., P .(1996)肌啡肽与癫痫。食物一般: 557 - 583。(Crossref)


